H2-Gehalt über das Oxidations-Reduktions-Potential (ORP) abschätzen
In vielen Angeboten von Geräten, die H2-Wasser erzeugen, hält jemand ein kleines Stabgerät mit einer digitalen Anzeige ins Wasser, auf der der direkt der H2-Gehalt des Wassers in ppm angezeigt wird (oder häufiger in ppb, weil eine tausendfach größere Zahl mehr Eindruck macht). Dabei handelt es sich jedoch nicht wirklich um eine Messung des H2-Gehalts, sondern schlicht um die Messung einer elektrischen Spannung, verursacht durch das Verhältnis unterschiedlicher negativ und positiv geladener Ionen im Wasser. Gemessen wird das "ORP" in Mikrovolt und daraus wird umgerechnet, wie viel gelöstes Wasserstoff-Gas im Wasser erforderlich wären, um diese negative Spannung im Wasser zu verursachen, zumeist noch nicht einmal über eine zusätzliche Messung des pH-Wertes und der Temperatur des Wassers korrigiert. Aber auch noch andere Inhaltsstoffe als H2-Gas können an dem negativen Redox-Potenzial beteiligt sein.
Daher ergibt diese "Messung" des H2-Gehalts im Wasser eher eine Hausnummer, die meist über dem realen H2-Gehalt liegt, als einen verlässlichen Wasserstoffgehalt. ![]() Hier ist sehr schön beschrieben, was es mit dem ORP des Wassers auf sich hat und
Hier ist sehr schön beschrieben, was es mit dem ORP des Wassers auf sich hat und ![]() hier etwas zur Beurteilung der so gewonnenen Ergebnisse.
hier etwas zur Beurteilung der so gewonnenen Ergebnisse.
Brauchbar ist diese Methode, um schnell zu erkennen, ob und wie schnell sich H2-Gas im Wasser löst, weil der Messwert dann entsprechend schnell in den Minusbereich sinkt. Beispiel einer ORP-Messung: 0,42 ppm H2, ORP -141, ph 8,5, 40,1 °C und gemessen mit den blauen Tropfen: 0,65 ppm H2
Geräte, die tatsächlich mit einem elektrischen Messfühler (einer kleinen Brennstoffzelle) den H2-Gehalt im Wasser messen können, sind wirklich sehr teuer, und der ebenfalls teure Messfühler muss immer wieder erneuert werden. Es wäre schön, wenn sich der H2-Gehalt so einfach und günstig, wie in der Werbung suggeriert, über das Redox-Potenzial messen ließe.
Alle Angaben zu H2-Messergebnissen auf diesen Seiten basieren auf der realistischeren Messmethode: den "blauen Messtropfen".
H2-Gehalt messen mit blauen Tropfen
Angeblich genau lässt sich der H2-Gehalt im Wasser mit dafür verkauften Messtropfen bestimmen. Die Verdünnung der Tropfen ist so eingestellt, dass jeder Tropfen in 6 ml des zu prüfenden Wassers genau 0,1 ppm an H2 bindet und sich dabei entfärbt. Ist alles H2 von den bisher eingetopften Tropfen gebunden worden, entfärbt sich der nächste Tropfen Methylenblau nicht mehr und das Wasser bleibt blau. Die Anzahl aller verwendeten Tropfen (incl. dem letzten Tropfen, der sich nicht entfärbte) mal 0,1 ppm ergibt dann, gemäß der den Tropfen beigefügten Anleitung, den gemessenen gewichtsmäßigen H2-Gehalt im Wasser in ppm.
Mit den blauen Tropfen wird nicht nur der Gehalt des Wassers an gelöstem Wasserstoff gemessen, sondern der Gesamtgehalt an H2-Gas, also auch das noch in feinsten Bläschen im Wasser schwebende H2-Gas. Möchte man den wahren Gehalt an gelöstem Wasserstoff messen, kann man das als einen Messfehler betrachten. Ein Hinweis darauf, dass ein großer Teil des im Wasser enthaltenen H2-Gases als Bläschen vorhanden ist, sich noch nicht gelöst hat, besteht darin, dass sich dann die Tropfen schneller entfärben, wogegen der Farbumschlag bei ausschließlich gelösten Wasserstoff ggf. langsamer erfolgt.
Geliefert wird meist eine kleine Flasche mit den blauen Tropfen und ein Messbecher mit Eichstrich, bis zu welchem meist 6 ml Wasser einzufüllen sind. Hilfreich zum Entnehmen und Abmessen des Wassers ist dabei eine 3 ml Einwegspritze (wie sie auch für die Spar-Variante der H2-Bestimmung verwendet wird).
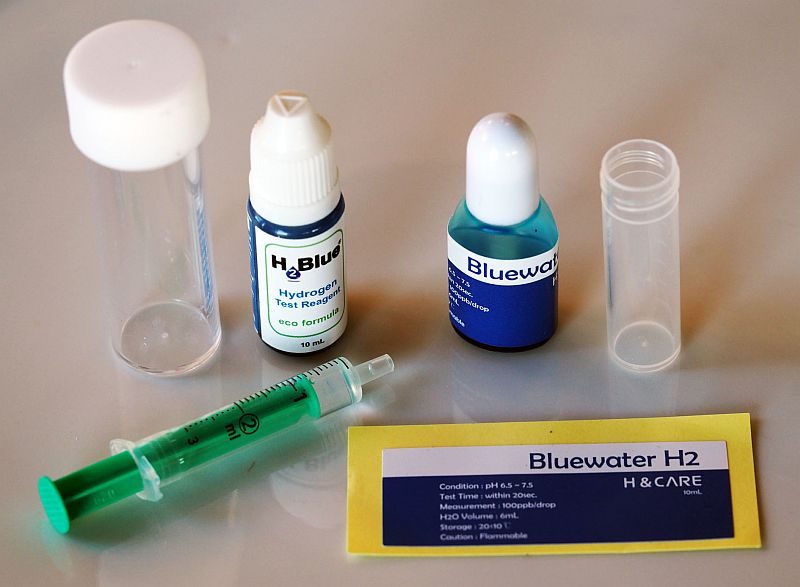
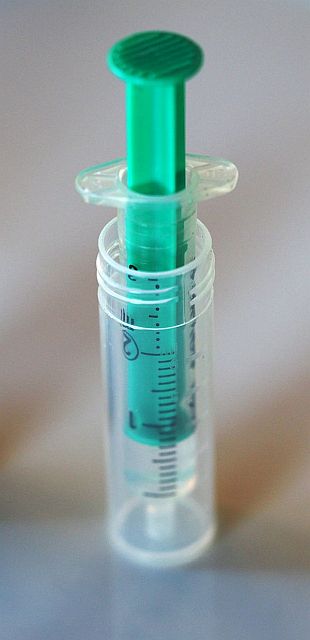
Bild: Das Produkt "Bluewater H2" ist inzwischen nicht mehr erhältlich.
Die Methode wird von den Herstellern der Tropfen als einfach, verlässlich und kostengünstig beschrieben. Die drei Versprechungen sollen im Folgenden mal näher beleuchtet werden.
einfach: So wie im Beipackzettel beschrieben ist die Methode auch einfach, denn Wasser abmessen und Tröpfchen-zählen kann wohl jeder.
Wichtig zu beachten und in der Anleitung nicht beschrieben: Die abreagierten Tropfen hängen nach dem Test an der Wandung des Messbechers und müssen vor dem nächsten Test sorgfältig entfernt werden. Deshalb das Gefäß nach jeden Test mehrfach spülen und mit Küchenpapier auswischen, oder so lange einweichen und Wasser wechseln bis das Wasser im Gefäß dauerhaft klar bleibt und sich nicht nach einiger Zeit wieder blau färbt.
Sehr einfach lässt sich damit aber Schaden durch dauerhafte Verfärbung anrichten, wenn etwas von den Tropfen daneben geht! Zur Sicherheit also immer auf mehreren Lagen Küchenpapier arbeiten!
Bei Verwendung der Spritze zum Einfüllen von H2-Wasser sehr langsam saugen und ausdrücken, weil Turbulenzen in der vorderen Verengung der Spritze schon wieder H2-Gas entweichen lassen können.
kostengünstig: Also billig sind die Tropfen wirklich nicht. Aber je nachdem, wie viel an kolloidalem Platin tatsächlich in den Tropfen steckt, mag der Preis gerechtfertigt sein. (25 ml Platin Nanopartikel-Dispersion mit 1 ppm an 3 nm großen Partikeln kosteten 2020 im Internet-Vertrieb 238 EUR, ist die Platin-Nanopartikel größer, ist die Lösung viel billiger ... hat bei mir aber nicht, mit Methylenblau und Alkohol (Ethanol) als Indikator funktioniert).
Hier beschreibe ich, wie sich bei geschickter Verwendung Tropfen einsparen lassen.
verlässlich: Dazu habe ich leider auch sehr schlechte Erfahrungen gemacht, und lange nicht gemerkt, dass die Messergebnisse schwanken und sehr oft daneben liegen.
Auf die Hersteller-Angabe, dass jeder "blauer Tropfen" der sich entfärbt, genau 0,1 ppm (bzw. 100 ppb) entspricht, ist überhaupt kein Verlass!
Die Tropfen sind ohne zusätzliche Überprüfung und ggf. Kalibrierung nur für Vergleichsmessungen im Sinne von "mehr" oder "weniger" H2-Gas zu gebrauchen. Vor jeder Messreihe sollten selbst ganz neue Tropfen unbedingt überprüft werden, ob sie auch tatsächlich einen plausiblen H2-Gehalt anzeigen! Ich hatte schon Tropfen, die einen nahezu doppelt zu hohen H2-Gehalt gemessen haben.
Hier beschreibe ich, wie sich das Verfahren so korrigieren lässt, dass die Messergebnisse auch mit "schlechten" Tropfen plausibel sind.
Hier wie sich die erreichte H2-Sättigung in % bestimmen lässt. (Diese Messmethode hat den großen Vorteil gut reproduzierbare Ergebnisse zu liefern, unabhängig von Wasserqualität, Luftdruck und Temperatur.